真空凍結乾燥工程におけるDSCの役割

多くのAPI(有効医薬成分)や製剤、特に生物製剤をベースにしたものは熱に敏感で水溶液中では不安定になります。特に後者の特性は、ワクチンの様な注入可能剤型の場合に、極めて不都合になります。より高い安定性と長い貯蔵寿命を達成するためには、このような医薬成分を乾燥させることが不可欠です。しかし、それらの熱不安定性のために、加熱だけで水分を除去することができません。フリーズドライや真空凍結乾燥は、熱処理無しにAPIやAPIと賦形剤の混合物を使用や貯蔵可能な形態に変換させる穏やかな乾燥法です。
真空凍結乾燥における3ステップ
凍結ステップ(初期乾燥と最終的な二次乾燥)
• 物質が選択された凍結速度で凍結される間の凍結ステップ
• 初期乾燥:氷は、減圧下の昇華によって凍結濃縮溶液から除去されます。この段階では通常、物質の温度は約-35 ℃から-20 ℃です。
• 二次乾燥:温度がさらに上昇され、マトリックス内に含まれる水の離脱によって、最終水分レベルまで物質が乾燥されます。安定したケーキを得るためには、1 %以下の水分濃度が必要です[1]。
医薬物質の実質的な損失を避けるために、通常、糖(例えば、ショ糖やトレハロース)やポリマーの様なクライオ、あるいはリオプロテクタントが添加されます。
凍結ステップ(初期乾燥と最終的な二次乾燥)
• 物質が選択された凍結速度で凍結される間の凍結ステップ
• 初期乾燥:氷は、減圧下の昇華によって凍結濃縮溶液から除去されます。この段階では通常、物質の温度は約-35 ℃から-20 ℃です。
• 二次乾燥:温度がさらに上昇され、マトリックス内に含まれる水の離脱によって、最終水分レベルまで物質が乾燥されます。安定したケーキを得るためには、1 %以下の水分濃度が必要です[1]。
医薬物質の実質的な損失を避けるために、通常、糖(例えば、ショ糖やトレハロース)やポリマーの様なクライオ、あるいはリオプロテクタントが添加されます。
崩壊温度
凍結乾燥工程のセットアップで決定的なパラメーターは、通常Tc と呼ばれる崩壊温度です。この温度で材料はそれ自身の構造を維持できなくなり、流動を開始するため溶解或いは軟化します。この理由から、物質は初期乾燥中、Tc 以下に保持するする必要があります。しかしながら、あまり低すぎるプロセス温度は、許容できないほど遅いプロセス進行につながります。結晶系では、最高許容温度は共融温度に対応しています[1 – 3]。この温度以下ではその系は完全に固体となります。
しかし、ほとんどの凍結乾燥された製剤には非晶質相が含まれており、このケースでは、崩壊温度は最大凍結濃度溶質のガラス転移温度(Tg´)に近くなっています。多くの場合、Tc は Tg´よりも少し高くなっており、両温度間の正確な相違は製剤によって変わります[2]。
凍結乾燥工程のセットアップで決定的なパラメーターは、通常Tc と呼ばれる崩壊温度です。この温度で材料はそれ自身の構造を維持できなくなり、流動を開始するため溶解或いは軟化します。この理由から、物質は初期乾燥中、Tc 以下に保持するする必要があります。しかしながら、あまり低すぎるプロセス温度は、許容できないほど遅いプロセス進行につながります。結晶系では、最高許容温度は共融温度に対応しています[1 – 3]。この温度以下ではその系は完全に固体となります。
しかし、ほとんどの凍結乾燥された製剤には非晶質相が含まれており、このケースでは、崩壊温度は最大凍結濃度溶質のガラス転移温度(Tg´)に近くなっています。多くの場合、Tc は Tg´よりも少し高くなっており、両温度間の正確な相違は製剤によって変わります[2]。
DSC (示差走査熱量測定)が Tg´を決定する
DSC測定装置は、ガラス転移を通過する間に起こるような材料の比熱容量の変化を検出するようデザインされています。
Fig.1は凍結した10 %ショ糖溶液の加熱中のDSC信号を示しています。冷凍と加熱は、この装置により5 K/minで実行されました。最大濃縮溶液の評価されたガラス転移温度(Tg´, ここでは中間点で評価)は-32 ℃となっており、文献値[4]と一致しています。吸熱ステップの高さはΔcpとして表示され、その量は0.28 J/(gK).となっています。
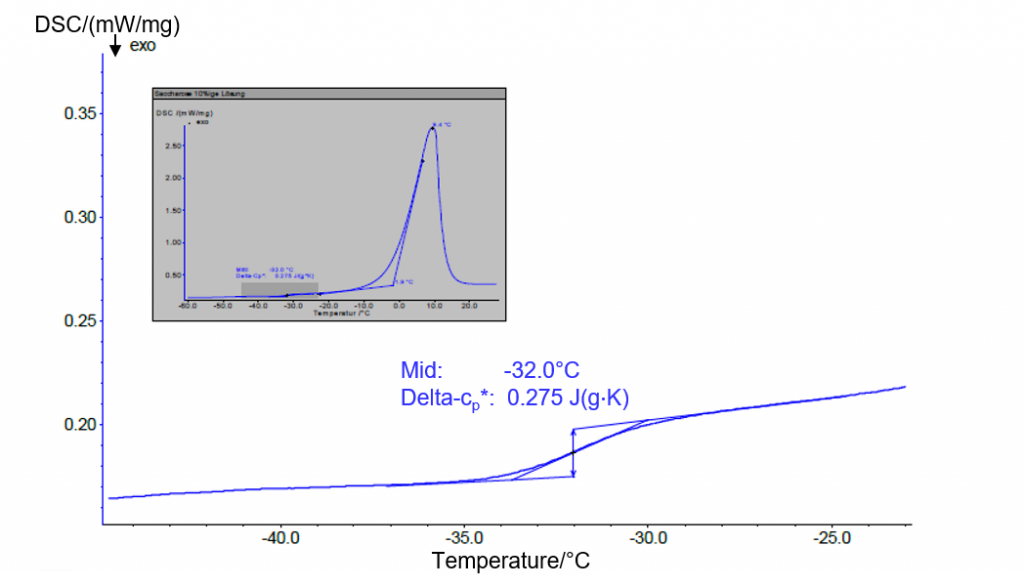
Fig.1:最大濃縮溶液のガラス転移;加熱速度5 K/min、密閉Alるつぼ
上述通り、多くの製剤でTg’は崩壊温度よりも少し低くなっていますので、これが最終製品品質に影響はないものの、保守的な上限温度を表しています。
ガラス転移ステップが、製剤組成の一つと関係する緩和反応や結晶化ピークと重なり合っている場合は、温度モジュレーションDSC (TM-DSCやmt-DSC)がその分離に役立ちます。
ガラス転移ステップが、製剤組成の一つと関係する緩和反応や結晶化ピークと重なり合っている場合は、温度モジュレーションDSC (TM-DSCやmt-DSC)がその分離に役立ちます。
乾燥製品のガラス転移温度
多くの凍結乾燥製品は乾燥後も非晶質形態を残しています。水は軟化剤効果を示すため非晶質相のガラス転移温度は捕らわれた残留水分と直接関係します。従って、DSCは材料の乾燥状態の解析にも使用することができます。
多くの凍結乾燥製品は乾燥後も非晶質形態を残しています。水は軟化剤効果を示すため非晶質相のガラス転移温度は捕らわれた残留水分と直接関係します。従って、DSCは材料の乾燥状態の解析にも使用することができます。
[1]E. Meister and H. Gieseler, A significant comparison between collapse and glass transition temperatures , European Pharmaceutical Review, online, September 2008
[2]V. Kett, Development of Freeze-dried Formulations Using Thermal Analysis and Microscopy , American Pharmaceutical Review, online, September 2010
[3]H. Schiffter-Weinle, Immer schön trocken bleiben , Deutsche Apothekerzeitung, online
[4]F. Franks, Freeze-drying of bioproducts: putting principles into practice , European Journal of Pharmaceutics and Biopharmaceutics, 1998, 45, p 221–229